Memahami air
Air merupakan suatu zat atau zat atau unsur yang penting bagi semua bentuk kehidupan yang diketahui sampai saat ini di Bumi. Air dalam bentuk cair merupakan senyawa yang tidak berwarna, tidak berbau, tidak berasa dan sulit dikompres yang memiliki beberapa sifat unik. Sifat air terdiri dari sifat kimia dan fisika.
Struktur dan komposisi air
Air adalah molekul sederhana yang terdiri dari satu atom oksigen yang terikat pada dua atom hidrogen berbeda. Karena keelektronegatifan lebih besar dibandingkan atom oksigen, maka ikatannya bersifat kovalen polar (ikatan polar).
Untuk setiap 1 molekul air, terdapat 2 atom hidrogen yang bergabung dengan 1 atom oksigen. Komposisi air atau bahan berair dapat diubah menjadi komponen dasarnya melalui proses elektrolisis. Elektrolisis adalah proses penguraian elektrolit (dalam hal ini air) menjadi komponen aslinya, oksigen dan hidrogen.
1 molekul air terdiri dari 1 atom oksigen dan 2 atom hidrogen.
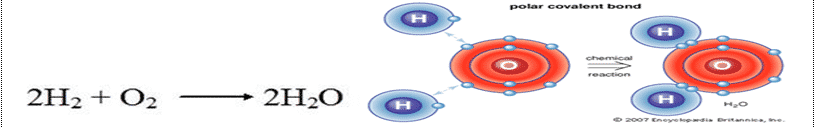
Dibutuhkan dua molekul gas hidrogen diatomik, yang bergabung dengan satu molekul gas oksigen diatomik untuk menghasilkan dua molekul air. Dengan kata lain perbandingan hidrogen dan oksigen adalah 2:1, perbandingan hidrogen dan air adalah 1:1, dan perbandingan oksigen dan air adalah 1:2.
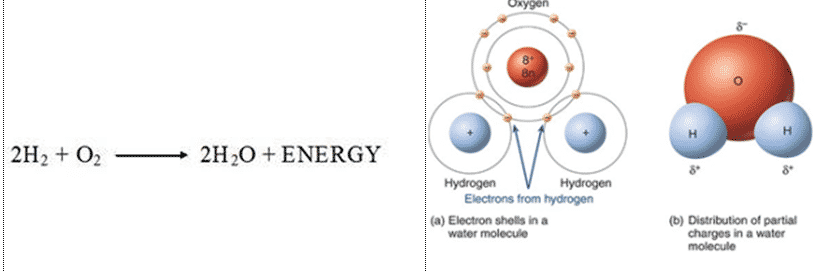
Sifat kimia air
Molekul air terdiri dari satu atom oksigen yang terikat secara kovalen dengan dua atom hidrogen. Hidrogen dan oksigen mempunyai daya gabung yang besar. Semua atom dalam molekul air disatukan oleh ikatan yang kuat, yang hanya dapat diputus oleh zat yang sangat agresif, misalnya menggunakan energi listrik atau bahan kimia tertentu.
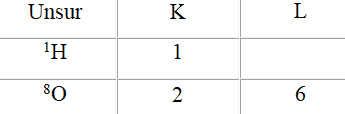
Sebuah atom oksigen (O) mempunyai inti dengan delapan proton pada orbital kulit K (2) dan L (6), sehingga tidak terisi dan memerlukan 2 elektron untuk kestabilannya. Sedangkan atom hidrogen (H) mempunyai kulit elektron tunggal dengan satu elektron di sekeliling intinya, sehingga masih kekurangan satu elektron. Kulit yang tidak terisi penuh berarti tidak stabil, sehingga elektron cepat bergabung dengan elektron lain untuk menstabilkan kulit, karena kulit yang terisi penuh merupakan bentuk stabil (orbital I stabil).
Sifat fisik air
Molekul air dapat dipecah menjadi unsur aslinya dengan mengalirkan arus listrik melaluinya. Proses ini disebut elektrolisis air. Di katoda, dua molekul air bereaksi dengan menangkap dua elektron, mereduksinya menjadi gas H.2 dan ion hidroksida (OH–). Sedangkan di anoda, dua molekul air lainnya membentuk gas oksigen (O2), melepaskan 4 ion H.+ dan mengalirkan elektron ke katoda. ion H+ Dan oh– mengalami netralisasi sehingga banyak molekul air yang terbentuk kembali.
Air adalah pelarut kuat yang melarutkan banyak jenis bahan kimia. Zat yang larut dan mudah larut dalam air (misalnya garam) disebut zat “hidrofilik” (suka air), dan zat yang tidak mudah larut dalam air (misalnya lemak dan minyak), disebut zat hidrofilik. zat (anti air). Kelarutan suatu zat dalam air ditentukan oleh mampu atau tidaknya zat tersebut menyamai kuat gaya tarik menarik listrik (gaya antarmolekul dipol-dipol) antar molekul air. Apabila suatu zat tidak dapat menandingi gaya tarik menarik tersebut antar molekul air maka molekul zat tersebut tidak akan larut dan akan beraspirasi menjadi air (Noor, 1990).
Air saling menempel (kohesi) karena air bersifat polar. Air memiliki muatan parsial negatif (σ-) di dekat atom oksigen karena pasangan elektron yang (hampir) tidak dipakai bersama, dan muatan parsial positif (σ+) di dekat atom oksigen. Dalam air hal ini terjadi karena atom oksigen lebih elektronegatif dibandingkan atom hidrogen, yang berarti ia (atom oksigen) mempunyai “gaya tarik” yang lebih besar pada elektron bersama dalam molekul.
menarik elektron lebih dekat ke dirinya sendiri (yaitu juga menarik muatan negatif elektron) dan membuat daerah sekitar atom oksigen lebih bermuatan negatif dibandingkan daerah sekitar dua atom hidrogen. Air juga mempunyai sifat kental karena sifat alaminya yang bersifat polar (Kay, 1966).
Air mempunyai tegangan permukaan yang besar karena sifat kohesif yang kuat antar molekul air. Hal ini dapat diamati bila sejumlah kecil air diletakkan pada permukaan yang tidak dapat dibasahi atau dilarutkan (tidak larut); Air akan terkumpul setetes demi setetes. Pada permukaan kaca yang sangat bersih atau mempunyai permukaan yang sangat halus, air dapat membentuk lapisan tipis (thin film) karena gaya tarik menarik molekul antara molekul kaca dengan air lebih kuat dibandingkan dengan gaya kohesif antar molekul air.
-
Struktur beku dan es
Molekul air dapat berikatan dengan empat molekul air dan membentuk kisi kristal heksagonal dalam es. Ciri penting lainnya dari ikatan hidrogen adalah bahwa ikatan ini terarah dengan baik sesuai dengan susunan orbital bersama antara atom hidrogen dan atom oksigen. Panjang ikatan hidrogen yang berbeda bergantung pada struktur geometri dan distribusi elektron.
Misalnya dalam bentuk es, setiap molekul air mempunyai panjang ikatan hidrogen sebesar 1,77 Å, setiap molekul air mempunyai ikatan hidrogen dengan 4 tetangganya dengan jarak oksigen ke oksigen sebesar 2,76 Å. adalah Å, sedangkan setiap molekul air mengandung hidrogen. Berikatan dengan 3 atau 4 molekul air lainnya. 15 dengan jarak oksigen-ke-oksigen 2,90 Å pada suhu 0C, dan 3,05 Å pada suhu 83 0C.
Air dapat membubarkan senyawa amfipatik (senyawa golongan hidrofobik dan gugus hidrofilik) yang molekulnya mengandung gugus polar, misalnya asam lemak. Contohnya adalah garam Na-oleat.
Natrium oleat mempunyai rantai hidrokarbon yang panjang sehingga dapat dikatakan sangat sulit terdispersi dalam air, namun nyatanya rantai hidrokarbon yang panjang ini terdispersi dalam air dan membentuk misel (di sini air yang bersifat polar tidak larut. Asam oleat mempunyai rantai hidrokarbon non-polar, sehingga terbentuk misel).
Dalam hal ini, gugus karboksil yang bermuatan negatif terlihat di permukaan sedangkan rantai hidrokarbon non-polar dan tidak larut berada di dalam. Dalam bentuk misel, terjadi tarik-menarik timbal balik melalui interaksi van der Waals, yaitu antara rantai hidrokarbon yang berdekatan, tarik-menarik ini disebut interaksi hidrofobik. Contoh lain komponen sel yang membentuk struktur nonpolar dengan bagian hidrofobiknya tersembunyi dari air adalah protein dan asam nukleat (Murray, 2006).
Elemen air
- Unsur-unsur penting dalam siklus hidrologi:
- Penguapan: Penguapan langsung dari badan air
- Transpirasi : Penguapan air pada tumbuhan
- Respirasi: Penguapan air dari tubuh hewan dan manusia
- Evapotranspirasi: Kombinasi evaporasi dan transpirasi
- Kondensasi : Proses perubahan wujud uap air menjadi butiran air akibat pendinginan.
- Presipitasi : Hujan atau segala bentuk presipitasi dari atmosfer ke permukaan tanah termasuk hujan, hujan es, salju.
- Infiltrasi: Air yang jatuh ke permukaan tanah dan meresap ke dalam tanah.
- Perkolasi: Air yang terus tenggelam hingga kedalaman tertentu hingga mencapai air tanah.
- Limpasan: Air yang mengalir melalui daratan menuju selokan, sungai, dan laut.
FTempat berlindung air
Berupa dispersi koloid, dimana partikel-partikelnya tidak larut atau larut. Senyawa protein yang dapat membentuk dispersi koloid Gelatin akan membentuk dispersi koloid bila ditambahkan air panas. Pada suspensi, partikel bahan berukuran lebih besar sehingga tidak larut dan membentuk koloid, misalnya pati dalam air dingin.
Air mendispersi/melarutkan berbagai zat berdasarkan sifat dipolarnya, seperti NaCl (membentuk ion), kemudian banyak zat yang tidak membentuk ion tetapi membentuk senyawa polar seperti aldehida, alkohol dan gula yang larut dalam air. Kelarutan zat-zat di atas disebabkan oleh adanya gugus hidroksil (alkohol dan gula) dan gugus karbonil oksigen (aldehida dan keton) (Kay, 1966).
-
Air adalah nutrisi terpenting bagi tubuh.
Manusia dapat bertahan hidup selama berminggu-minggu tanpa makanan, namun hanya beberapa hari tanpa air. Tubuh manusia terdiri dari 55-75% air. Air adalah salah satu bahan pembangun dasar darah, enzim pencernaan, urin, keringat, dan bahkan jaringan otot, lemak, dan tulang.
Karena tubuh tidak dapat menyimpan air, maka kita memerlukan air segar untuk menggantikan air yang dikeluarkan dari berbagai organ vital tubuh melalui keringat, urin, feses, dan lain-lain. Banyaknya air yang kita butuhkan tergantung pada metabolisme tubuh, suhu udara, cuaca, makanan yang kita makan dan tentunya tingkat aktivitas kita (Winarno, 1989).
Air berperan sebagai bahan yang dapat mendispersikan berbagai senyawa yang ada pada bahan tersebut. ion H+ Dan oh ion-ionnya– Ini sebenarnya menentukan sifat biologis dan struktur molekul yang dikandungnya, seperti protein, lipid dan komponen sel lainnya (Girindra, 1986).
Senyawa air
Kandungan senyawa kimia penting dalam air laut (garam air garam = 35%)
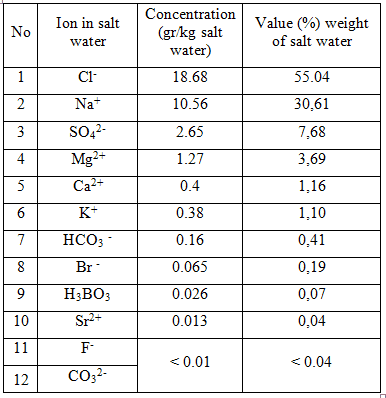
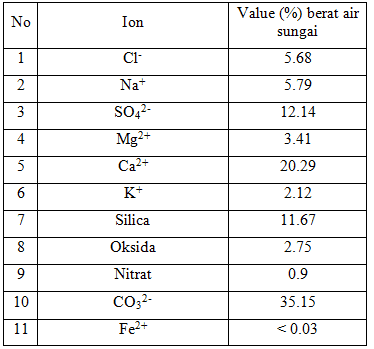
. Kandungan senyawa kimia penting dalam air sungai
Demikian artikel dari duniapendidikan.co.id Apa Fungsi Air Bagi Manusia : Komposisi, Sifat, Kimia, Pengertian, Unsur, Senyawa, semoga artikel ini bermanfaat bagi anda semua.



